һ��iga�������߿�pla2r��������Ѫ˨Ѫ�ܲ��ĺ�������
��ѧȺ�����ɭ������
�Ĵ�ʡҽѧ��ѧԺ•�Ĵ�ʡ����ҽԺ�����ӿƼ���ѧ����ҽԺ��
����ժҪ��
���ߣ�Ů��26�꣬�������ָ��������쳣1�꣬��֫ˮ��3������Ժ��2024��9��ͻ����ʶɥʧ���鴤������ҽԺ��Ѫѹ180/140mmHg�����������쳣�����ƺ��ת����Ժ�����������������Բ����ι��ܲ�ȫ�������ܲ�ȫ�ȣ�����ǿ���ɵȡ�9��26������Ժ���ڿƣ�ͷMRIʾ�Ҳ��ҶСȱѪ����ܣ��������ݲ��㣬ͣ��ǿ���ɡ�9��27�������渡�ף�Ѫѹ200/138mmHg��Ѫ����198.3��mol/L��eGFR 29.6ml/min������29.8g/L����2+����ACR 2164��g/mg��ת���ҿƣ�10��8�������ʾIgA���������������Բ���鼱����С�����ˣ�����Ժ����������30mg/d������ͣ�ã��ڼ䷴����ð��������ʹ��������̩�����գ�δ���ɸ��2025��7�³�����֫ˮ�ס�Ƥ��������������������ԡ����٣�δ��ʱ���2025��10��14����֢״���أ�Ѫ����660.4��mol/L�ٴ���Ժ������ʷ�������ż��֣�����Ӧ��Ƥ�ף��������ȵ�����������飺T 36.5����P 97��/�֣�R 20��/�֣�BP 149/87mmHg�����渡�ף�ȫ������ɫƤ�����м��˫��ϸʪ�������ϸ���ѹʹ��˫��֫ˮ�ף�������������㼰���ܶˮ�塢Ѫ�壬��˫��֫ɢ��ˮ�塣
������飺
ʵ���Ҽ����Ѫ���棺Hb 72g/L ����PLT 73��10⁹/L ����WBC��NEUT�������������������� 31.45 mmol/L �������� 671.5 ��mol/L �������� 506 ��mol/L ������ 5.48 mmol/L ������ 3.50 mmol/L �������� 29.2 g/L ����LDH 394 U/L ����AST��ALT��������Ѫȫ��δ���쳣����Ѫ������FIB 1.51 g/L ����D-������ 1.30 mg/L ����PT�������ļ�����ָ�꣺hs-cTnT 40.00 ng/L ����BNP 1376 pg/mL ������ϸ����̬����Ƭ��ϸ������2.8% ������ϸ����̬��С���ȣ��ɼ���ϸ����Ƭ�����Ρ�����Ρ���Բ�κ�ϸ��������ѧ��飺������֬����IgA ��������2GPI IgM/IgA ������2024-09����PLA2R-IgG 89.3RU/mL ������2025-10-17����PLA2R-IgG 210.58RU/mL ������Һ�����������������ʡ���k/����ֵ���������崯��ؿ���Dsg1��Dsg3��BP180���������ANA���ԣ�1:100������2024.10.12������C3 0.348 g/L �����������C4������ϸ�����ߣ�CD4+�ܰ�ϸ�� 256/uL ��, B�ܰ�ϸ��12/uL �������߹̶���Ӿ��Ѫ�嵰��Ӿ������ο��塢ANCA����GBM���塢��dsDNA���塢��CCP���塢�Ǵ��������δ�������쳣��ADAMTS13�����������������Կ������ԡ���״�ٹ�����TSH 14.10 mIU/L ����FT3��FT4��������״�ٿ������ԡ���״���ټ��أ�PTH 139.0 pg/mL����ƶѪ��ش�л���������747.25 ng/mL����Ҷ��2.6 ng/mL ����ת�����ױ��Ͷ�62.8% ����Ѫ�����������32 umol/L �����������������11.6 umol/L �����ĵ�ͼ����������쳣������ϵ������飺˫��ʵ�ʻ�����ǿ��Ƥ���ʷֽ粻�壬����ϵͳ�����롣CDFI��ʾ˫��Ѫ����ע����೬��������������������ȹرղ�ȫ���������ȹرղ�ȫ���������-�жȹرղ�ȫ���ζ��������������ζ���ѹ���ߡ���ǻ���������ʽ��ͣ���ʾ���ҷ�ѹ���ߣ��������İ���Һ���ظ�ˮ��������ʾ˫����ǻ��Һ����ǻ����ǻ��Һ���ز�CT����2024-11-25��Ƭ�Աȣ���1��˫��ɢ�ڶĥ��������ڡ�Ƭ��Ӱ����ǰ��������Ⱦ�Բ�����ܣ������ٴ���2.˫��ɢ�ڶ��ʵ�Խ�ڣ��������Կ��ܣ���ǰ���������3.�Ҳ���ǻ������Һ����ǰ���ࣻ�����ǻ������Һ����ǰ���٣��ҷ���Ҷ����ʵ�䡢���š�4.�ݸ��ܰͽ��Զࡣ5.�����������¶������ζ����������֡��İ�������Һ����ǻ�ܶ��Լ��ͣ�ƶѪ�������ٴ���6.�ر�����֯���͡�ɨ������ƻ���
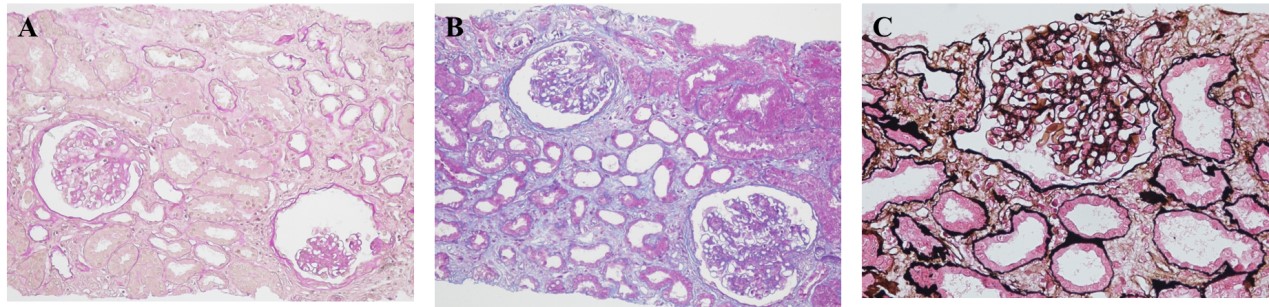
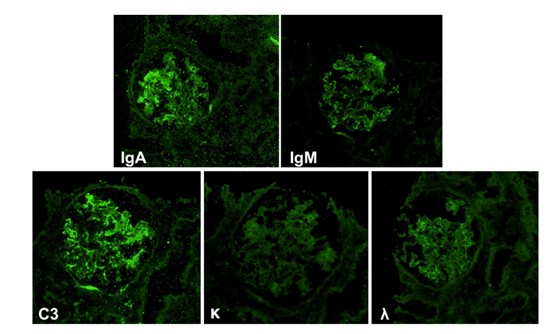
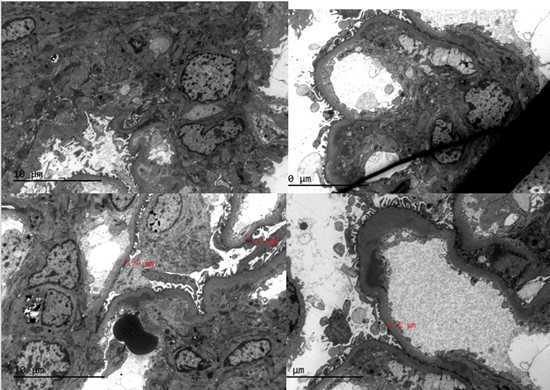
����֯�������1���⾵�����ͼ1�����¼�2��Ƥ��������֯����Ⱦɫ��Ƭ�ɼ�6����С�����д�С��������������С������ϸ�������࣬С��ϵĤϸ���ͻ���������������ڶ�����һ�ض���������ϵĤ���ɼ�2~4��ϵĤϸ�����ڶ�ϵĤ������������Ĥδ�����Բ��䣬������ϸѪ��ǻ��խ���ڶ�ëϸѪ����ϸ�����࣬�ڶ�ϵĤ���ɼ��ȸ��쵰�׳����ɼ�1��С�������ճ������С����Ƥϸ�����ݼ��������ԣ���״��С����Ƥϸ����ƽ��ˢëԵ������ǻ���ţ���������С��ή����������ά����Լ10%�����ɼ���ϸ�������γɣ������ʾ�����ˮ�ף��������ܰ͡�����ϸ����������ϸ������Լ5~10%��������С�����ܱ����������ɼ����������ԡ���2������ӫ������ͼ2�����¼�1����С��IgG����IgM����IgA����������C3������C1q����FRA-��A1b-���ʡ���������PLA2R-��ϵĤ����״��������3���羵�����ͼ3�����¼�1����С��ϵĤ�����ڶ�����~�ж�������ϵĤ�������࣬ϵĤ����ϵĤ�����ɼ�������״���������������ëϸѪ��ǻ���ڶ�����խ��������Ƥϸ�����ݱ��ԣ�����Ĥ���������ڶ���Ƥ�¿ɼ����������������������ϸ������ͻ���ںϣ���С�ܼ����ʣ�������С����Ƥϸ����ë���䣬������������ԭ��ά�����������ܰ�ϸ��������ϸ������
ͼ 1 �����⾵��顣A HEx200��B PASx200��C PASMx200
ͼ 2 ���������ӫ���顣
ͼ 3 �����羵���(x2000)
��ϼ��������
�����1��IgA��������PLA2R�������ԣ� ���������ܲ�ȫ���Լ��أ�2��Ѫ˨Ѫ�ܲ� �ǵ�����Ѫ�����ۺ�����3����������˥��ʧ������4����л���Բ� �����������5��Ƥ����Ⱦ ���崯��6����Ѫѹ3�� ����Σ��7���ཬĤǻ��Һ(��ǻ��Һ����ǻ��Һ��ǻ��Һ�İ���Һ)��8���β���Ⱦ��9��������Ѫ֢��
���������1��Ĥ��������������������������Ѫ�忹PLA2R�������ԣ�������֯������֧�֡�2����Ⱦ��������ף������������ϲ���Ⱦ����Ȼ������һ�����½��������ಡ����֧�֡�3��TTP���û��������ܽ������½���ƶѪ��PLT�½���LDH���ߣ���������ϸ������ADAMTS13����������112.38%�������������ԣ��ų�TTP��
���Ƽ�ת��
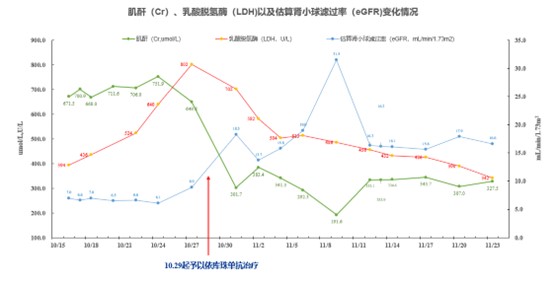
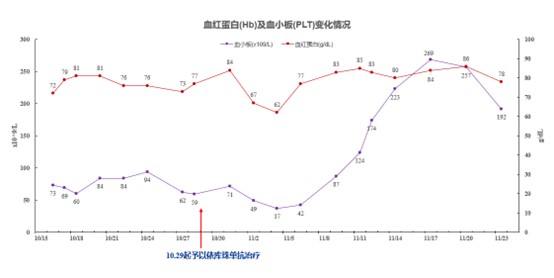
��Ժ�����Լ���40mg qd��3�ܺ�������Ƭ25mg qdά�֣�ͬʱ������������0.5g q12h��ѪҺ����ѪҺ���˹����������������̹�������ù�ؿ���Ⱦ����ѹ����֬��������ȶ�֢֧�����ơ��������������ܲ�ȫ���Լ��أ�ƶѪ��ѪС�彵�ͣ�LDH���������ߣ�����ѪͿƬ�������ϸ�������Ѫ˨Ѫ�ܲ���ȷ������ADAMTS13 ����112.38%�������Կ������ԣ���ϲ�ʷ���ʿ��Ƿǵ�����Ѫ����֢�ۺ�����aHUS������10-29��11-05��11-08�ֱ�����ע�����鵥��600mg���ơ����ƺ�����ˮƽ�����½���LDH�½���Hb��PLT���ƣ������ֱ���11-15��11-22������ע�����鵥��900mg��ͼ4��5��6����
ͼ 4 �û���������������ø����С���˹��ʵı仯�����
ͼ 5 �û���Ѫ�쵰��ѪС��ı仯�����
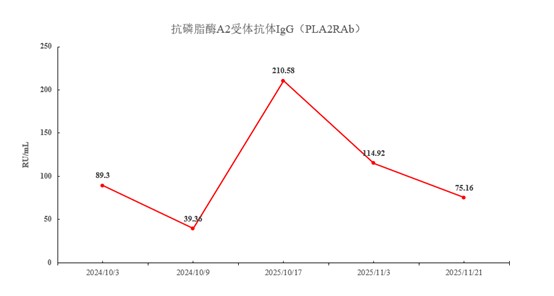
ͼ 6�û��ߵĿ�PLA2R����ı仯�����
����
���ı�����һ��IgA������������֮�����ڲ�����������ΪIgA��������Ѫ�忹PLA2R����Ϊ�����Ҳ����кϲ�Ѫ˨Ѫ�ܲ�������Ϊ����Ů�ԣ����̳������裬������Ϊ��ϵͳ֢״�����ڼ�������������������Ƿ�淶��δ������ã������չѸ�٣������ܿ��ٶ��ϲ�֢�࣬������Ӧ��Ƥ�Ƥ�����崯����Ⱦ��Ѫ˨Ѫ�ܲ�����ϵͳ����ʹ��Ϻ�������Ϊ���ӡ��ڼ�Σ��֢�����£���ο���ʶ����жϲ��������������Ƽ�����ʱ����ǿ�ȣ��Ǹò��������ٴ��Ĺؼ���ս�����Ľ������ϰ��̽�ָú��������Ŀ��ܻ��ƺ����Ʋ��ԡ�
������ϣ��û�����Ҫ������IgAN��MN��IgA�����ϲ�Ĥ��������cIgAN/MN����ԭ����Ĥ��������IgAN��Ȼ��Ϊ���߸�����鵼����С�������������߷������Ʋ�ͬ����ͬ������ͬһ���߲��������IgAN���ص�������С���г���IgA���߸����������֢������ ADDIN EN.CITE ADDIN EN.CITE.DATA 1����MN���������С����п�ԭ�����߸������γ����£�������С�����Ĥ(GBM)���������������䲡����������Ϊ������G��ԭ����Ĥ��������Ҫ��IgG4������֬øA2���壨PLA2R�����������Ͷԭ���߸������FCN3��CD206��EEA1�ȣ���Ⱦɫ���� ADDIN EN.CITE ADDIN EN.CITE.DATA 2,3��cIgAN/MNָͬһ��������첡����ͬʱ����IgAN��MN����ԭ������С���IJ����ı䡣���Ա�����ѧ��һҽԺ���������������137������cIgAN/MN�о�����IgAN��ȣ�cIgAN/MN���ٴ��������������������������־��ˮƽ�ͼ����������Ŵ����յȷ������������MN���� ADDIN EN.CITE ADDIN EN.CITE.DATA 4��������ǵIJ������з������û�����С���ڴ���ϵĤIgA��������û����Ƥ��IgG��������֯ѧ��PLA2R���ԣ�������MN����ϣ�������ǽ���������ȷ��Ϊ�����Ѫ�忹PLA2R�������Ե�IgA�������ߡ�
�Ƿ�PLA2R�������Ի�Ӱ��IgA�������ߵ�Ԥ��PLA2R����I�Ϳ�Ĥ���壬��������С���зֲ�����ϸ���� 5,6��PLA2R������������С���б���ϵͣ���ϵĤ��������С������ʵ��ģ���б����ϵ�7������2009����о��У���M��PLA2R��ΪMN����Ҫ�е�8����PLA2R����IJ���������Ҫ���Ŵ��б����£����������շ�����Ӧ������PLA2R������ı䣬��¶�¿�ԭ��λ����������Ӧ������������塣��������ϸ��PLA2R��Ϻ�ͨ�����鵼���������ñ�����ϸ���ڲ���������ø�彵�⡣�����������PLA2R�Ķη�����ǿ�˿�ԭ�ʵݣ��ٽ�CD4⁺Tϸ����������̼�Bϸ����������壬�γɶ���ѭ��9,10���о����ֶԿ�PLA2R����Ķ������������������������ƽ���ʱ���������ʧ���ڻ���Ŀ�ʼ���ҿ�PLA2R����ij�����������Ԥʾ�Ų����Ľ��11,12��ͬʱ���ڿ�PLA2R����ˮƽ���ͺ�����Ҳ������13����ˣ�Ŀǰһ������Ϊ��PLA2R����ζȱ仯��MN�����ٴ������Ʒ�Ӧ�Լ�Ԥ��������ء�Ȼ������PLA2R���������Ƿ�Ҳ��Ӱ��IgA�������ߵ�Ԥ��Ŀǰ��ȱ�������ٴ�����Ԥ��֤�ݡ�
ֵ��ע����ǣ��û�����ƶѪ��Hb72g/L����ѪС����٣�73x10⁹/L������β���Ѻ�ϸ����LDH�����Լ�������˥�ߵı��֣�����Ѫ˨Ѫ�ܲ�����ϡ�����ADAMTS13����112.38%�������Կ������ԣ���ʾ�û��߿����Ƿǵ�����Ѫ����Ѫ֢��aHUS����aHUS�γɻ�����Ҫ�����Ŵ��еĻ����ϣ��ɴ��������շ������²������;��ʧ�ؼ����������Ѫ����Ƥ���˺Ͷ�����Ѫ˨�γ�14���ں�������������Ҫ���Dz���C5���Ƽ����������鵥��������15�������鵥��ͨ�����Ʋ��弤��������Ը���aHUS��ص���Ѫ�����������ˣ�����Ӿ���ȫ�����Ȼ������״̬���������������壨������PLA2R���壩���쳣��������������ζ��½�16���ź�������������õ�ԭ��û�����Ʋ���������ӵļ�顣�������ϣ����Ǹ��ݲ������ʹ�������鵥�����ƣ�����ƶѪ��PLT���ٵõ����Ը��ơ�
�û����г��ڵ���Ӧ��Ƥ�ף����о���������֢��Ƥ������Ҫ�����Ƿ����������������м�����ߵ���������17�������������ǵ�˼�������ߵ�Ƥ���뱾�����崯��Ƥ����Ⱦ��IgAN�Ƿ������ϵ��ͨ���������ף����о���ʾ����Ӧ��Ƥ�������ڣ�����IgA1�����ǻ����������ؼ�ø��GALNT12��C1GALT1C1�ı���ˮƽ�������ڽ����ˣ���ø��ֱ�ӵ��°�����ȱ�ݵ�IgA1��Gd-IgA1���������ӣ���Gd-IgA1���Ǵ���IgA�������߸���������������������˵ĺ�����Ԫ����18,19�������Ӧ��Ƥ���ܻ�����IgAN�ķ��ա��������У��û��߳��ڵ�������Ƥ�����յ���Gd-IgA1�����������շ���IgAN��
�û����ٴ����ּ�Σ�أ������DZ���������һ�ѵ㡣�ڷ����ϣ�����ȷ�������е���������������������������IgA������ͬʱ��Ը������ߵIJ���֢���缱����˥����Ѫѹ��Ƥ����Ⱦ��������ȣ�����ѪҺ������ѹ������Ⱦ�ͽ�����ȶ�֢���ơ�����Ҫ���ǣ����ǵ�����aHUS���ж�ϵͳ���۰�����ϵͳ��������ѪҺϵͳ�ȣ����Ǹ�����Ѫ���û��������鵥�����ƣ����ƺ��ߵ������ܡ�ƶѪ��ѪС���ָ���ת�����岡��õ��˼�ʱ�Ŀ��ơ�
�������������ı���һ��������Ѫ�忹PLA2R�������Ե������ȷ��ΪIgAN�IJ�����Ϊδ���ٴ��о��ṩ�˱�����ٴ����ϣ�ҲΪ���������С���������ṩ����Ҫ��ʾ�����ȣ�����ϲ����ϣ�Ӧ��ֲ���ѧ����������ƾѪ��ѧ���Բ������ΪIgA������Ĥ�������ĺϲ�֢���ò�����ʾ���������Ʋ��Լ�Ԥ�����������ԭ������С�������䵱Ѫ��ѧ�벡��ѧ�����һ��ʱ�������̻�����Ǽ�����ϲ��ɻ�ȱ�����ݡ���Σ����ٴ������ϣ�Ӧ����DZ����ز�ʷ���ھ��⣬�������ߺϲ���Ӧ��Ƥ�ף���ʾ�������ƻ���Ƥ�������ܶ��ӻ�IgA�����ķ������չ����DZ�ڼ�ֵ��
���ο����ס�
1 Zhao, J., Ma, F., Bai, M. & Sun, S. Low-Dose Corticosteroid Combined With Mycophenolate Mofetil for IgA Nephropathy With Stage 3 or 4 CKD: A Retrospective Cohort Study. Clin Ther 43, 859-870, doi:10.1016/j.clinthera.2021.03.009 (2021).
2 Caza, T. N. et al. Discovery of seven novel putative antigens in membranous nephropathy and membranous lupus nephritis identified by mass spectrometry. Kidney Int 103, 593-606, doi:10.1016/j.kint.2023.01.001 (2023).
3 Dantas, M. et al. Membranous nephropathy. J Bras Nefrol 45, 229-243, doi:10.1590/2175-8239-JBN-2023-0046en (2023).
4 He, J. W. et al. Concurrent IgA Nephropathy and Membranous Nephropathy, Is It an Overlap Syndrome? Front Immunol 13, 846323, doi:10.3389/fimmu.2022.846323 (2022).
5 East, L. & Isacke, C. M. The mannose receptor family. Biochim Biophys Acta 1572, 364-386, doi:10.1016/s0304-4165(02)00319-7 (2002).
6 Lambeau, G. & Lazdunski, M. Receptors for a growing family of secreted phospholipases A2. Trends Pharmacol Sci 20, 162-170, doi:10.1016/s0165-6147(99)01300-0 (1999).
7 Beck, S. et al. Upregulation of group IB secreted phospholipase A(2) and its M-type receptor in rat ANTI-THY-1 glomerulonephritis. Kidney Int 70, 1251-1260, doi:10.1038/sj.ki.5001664 (2006).
8 Beck, L. H., Jr. et al. M-type phospholipase A2 receptor as target antigen in idiopathic membranous nephropathy. N Engl J Med 361, 11-21, doi:10.1056/NEJMoa0810457 (2009).
9 Sethi, S. & Fervenza, F. C. Antigens in membranous nephropathy: discovery and clinical implications. Nat Rev Nephrol 21, 653-670, doi:10.1038/s41581-025-00980-z (2025).
10 Liu, Y. et al. Antibody-induced internalization and degradation of PLA2R amplifies CD4(+) T cell activation. Theranostics 16, 37-57, doi:10.7150/thno.123035 (2026).
11 Beck, L. H., Jr. et al. Rituximab-induced depletion of anti-PLA2R autoantibodies predicts response in membranous nephropathy. J Am Soc Nephrol 22, 1543-1550, doi:10.1681/asn.2010111125 (2011).
12 Dahan, K. et al. Rituximab for Severe Membranous Nephropathy: A 6-Month Trial with Extended Follow-Up. J Am Soc Nephrol 28, 348-358, doi:10.1681/asn.2016040449 (2017).
13 Ruggenenti, P. et al. Anti-Phospholipase A2 Receptor Antibody Titer Predicts Post-Rituximab Outcome of Membranous Nephropathy. J Am Soc Nephrol 26, 2545-2558, doi:10.1681/asn.2014070640 (2015).
14 Bogdan, R. G. et al. Atypical Hemolytic Uremic Syndrome: A Review of Complement Dysregulation, Genetic Susceptibility and Multiorgan Involvement. J Clin Med 14, doi:10.3390/jcm14072527 (2025).
15 [Multidisciplinary consensus on the diagnosis and treatment of atypical hemolytic uremic syndrome (2025 version)]. Zhonghua Nei Ke Za Zhi 64, 396-411, doi:10.3760/cma.j.cn112138-20250219-00095 (2025).
16 Cofiell, R. et al. Eculizumab reduces complement activation, inflammation, endothelial damage, thrombosis, and renal injury markers in aHUS. Blood 125, 3253-3262, doi:10.1182/blood-2014-09-600411 (2015).
17 Grandinetti, V. et al. Renal dysfunction in psoriatic patients. G Ital Nefrol 37 (2020).
18 Cao, W. & Xiong, J. Causal associations and potential mechanisms between inflammatory skin diseases and IgA nephropathy: a bi-directional Mendelian randomization study. Front Genet 15, 1402302, doi:10.3389/fgene.2024.1402302 (2024).
19 Li, C., Wang, B., Han, T., Xu, Y. & Li, X. Causal relationship between inflammatory skin diseases and immunoglobulin A nephropathy: A Mendelian randomization and enrichment analysis study. Skin Res Technol 30, e13915, doi:10.1111/srt.13915 (2024).